西达本胺(Chidamide;商品名:爱谱沙®/Epidaza®)是公司独家发现的新分子实体药物,机制新颖,是全球首个亚型选择性组蛋白去乙酰化酶(HDAC)抑制剂和全球首个获批治疗外周T细胞淋巴瘤及晚期激素阳性乳腺癌的口服治疗药物,属于表观遗传调控剂类药物。
西达本胺作用于表观遗传相关靶点—组蛋白去乙酰化酶(第I类的1、2、3亚型和第IIb类的10亚型)。组蛋白去乙酰化酶(HDAC)是一类对染色体的结构修饰和基因表达调控发挥重要作用的蛋白酶,西达本胺作为HDAC抑制剂,通过抑制HDAC的生物学活性产生作用,并由此产生针对肿瘤发生的多条信号传递通路基因表达的改变(即表观遗传改变)。
具体而言,西达本胺的一般性作用机理主要包括:①直接抑制肿瘤细胞周期并诱导细胞凋亡;②诱导和激活自然杀伤细胞(NK)和抗原特异性细胞毒T细胞(CTL)介导的肿瘤杀伤作用;③抑制肿瘤细胞的表型转化及微环境的促耐药/促转移活性。
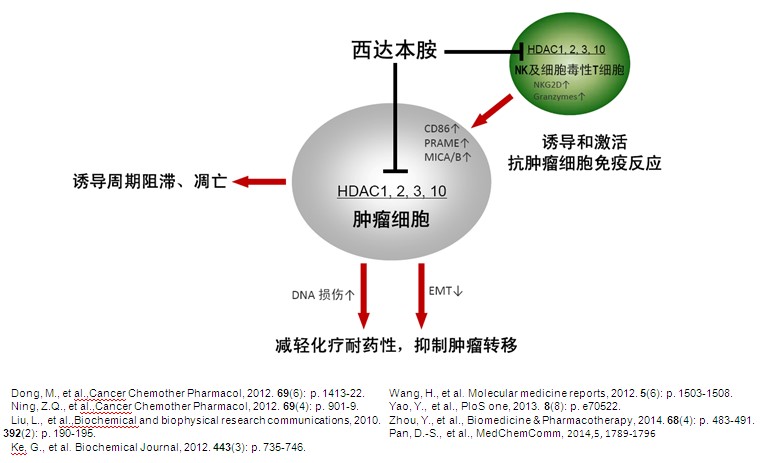
图 西达本胺(爱谱沙®)抗肿瘤分子作用机制
- 2014年12月,中国获批用于既往至少接受过一次全身化疗的复发或难治的外周T细胞淋巴瘤(PTCL)患者,填补了我国该治疗领域空白。
- 2017年7月,被纳入国家医保,惠及更多患者。
- 2019年11月,中国获批联合芳香化酶抑制剂用于治疗雌激素受体阳性、人表皮生长因子受体-2阴性、绝经后、经内分泌治疗复发或进展的局部晚期或转移性乳腺癌患者。首次确证HDAC抑制剂联合其他靶向药物可有效改善肿瘤耐药,成为全球首个以实体肿瘤为适应症获批的表观遗传调控机制类药物。
- 2021年6月,日本获批单药用于治疗复发性或难治性(R/R)成人T细胞白血病(ATL)患者。
- 2021年12月,西达本胺在日本获批第2个适应症——单药用于治疗复发性或难治性(R/R)外周T细胞淋巴瘤(PTCL)患者。
- 2023年3月,中国台湾获批用于治疗荷尔蒙受体阳性且第二型人类表皮生长因子接受体(HER2)阴性,且经内分泌治疗后复发或恶化之停经后局部晚期或转移性乳腺癌患者(联合依西美坦)。
- 2024年4月,中国获批联合R-CHOP(利妥昔单抗、环磷酰胺、阿霉素、长春新碱和强的松)用于治疗MYC和BCL2表达阳性的既往未经治疗的弥漫大B细胞淋巴瘤(DLBCL)患者。
- 2024年12月,西达本胺弥漫大B细胞淋巴瘤(DLBCL)适应症首次纳入国家医保目录。
全球范围其他适应症探索情况:
- 2024年3月,由中山大学肿瘤防治中心徐瑞华教授、王峰教授牵头开展的CAPability-01研究荣登全球顶尖学术期刊《Nature Medicine》(IF=82.9)。该研究显示,对于微卫星稳定或错配修复功能完整(MSS/pMMR)型转移性结直肠癌(mCRC)患者,西达本胺+信迪利单抗+贝伐珠单抗三药方案进行三线及以上治疗18 周PFS 率达64.0%,ORR 达 44.0%,中位 PFS 达 7.3个月,是MSS/pMMR 晚期mCRC 患者极具前景的治疗选择。2024年6月,该适应症被国家药品监督管理局药品审评中心(CDE)正式纳入“突破性治疗品种”。2024年7月,西达本胺联合信迪利单抗和贝伐珠单抗治疗≥2线标准治疗失败的晚期微卫星稳定或错配修复完整(MSS/pMMR)型结直肠癌患者的III期临床试验申请获批准,计划共入组430例,截至2025年4月,已完成200例入组。
- 2024年 11月,西达本胺联合CHOP用于初治、具有滤泡辅助T细胞表型外周T细胞淋巴瘤(PTCL-TFH)的随机、双盲、安慰剂对照、多中心、III期临床试验申请获受理,并于2025年2月获得临床试验批准通知书。
- 公司国际合作伙伴HUYABIO(沪亚生物国际)在全球17个国家开展的西达本胺联合纳武利尤单抗一线治疗晚期黑色素瘤的随机、双盲、阳性对照III期临床试验完成入组。HUYABIO在2024年癌症免疫治疗学会(SITC)年会报告了西达本胺联合纳武利尤单抗一线治疗黑色素瘤的II期临床试验随访结果,在39例患者中ORR达65.8%,CR达15.8%,mPFS达36.9月,展现优异的疗效潜力。
- 此外,公司正在开展西达本胺单药、联合免疫治疗或其他药物在血液肿瘤、实体瘤等多项研究者发起的临床研究。
详细信息,敬请访问爱谱沙产品网站(www.epidaza.com),也可扫描下方二维码,关注【深圳南宫NG·28生物科技股份有限公司】&【爱谱沙医学信息平台】,获取最新产品资讯。




